News Detail
 来源:本站
来源:本站
 浏览量:11110
浏览量:11110

提到心脏安全性风险,hERG这个小机灵鬼就会出现人们头脑中,而对于抗肿瘤药物,人们也总能发现一些 “例外”:
Osimertinib (奥希替尼) 检测hERG-IC50是0.69 µM;
Entrectinib (恩曲替尼) 检测 hERG-IC50是0.60 µM,2021-08-19获得FDA批准。

我们在工作中也时常遇类似以下的提问:
肿瘤药物研发中体外实验的心脏安全性,是否也是聚焦于hERG 以及 QT 延长?是否还有其他需要的考量?是否对于肿瘤药物的心脏安性容忍度更大?
那么,我们就基于现有的文献报道和工作实践,简单聊聊这个话题。

Part-1:心脏安全性是肿瘤药物开发中必须面对的风险。
2017年十月24-25日,在位于美国 Silver Spring的FDA总部,举办名为 ”Detection, Assessment, and Risk Mitigation of Cardiac Safety Signals in Oncology Drug Development”的研讨会,把肿瘤药物开发中心脏安全性的问题,提到了人们面前。
“这是一个对治疗肿瘤药物研究而言充满了希望的时代:截至2018年5月,仅美国公司开发的抗癌症药物和疫苗就超过了1100种。肿瘤相关药物占据了全球临床研究管线的40%,约有1600种产品。在过去几年中,全球已经推出了超过60种抗癌症药物。癌症患者的死亡率在过去20-30年中大幅下降,癌症患者的存活期也大大提高。” – 接下来的是一个血红色的但是:
“抗肿瘤药物的心血管毒性是也是极为显著的:文献据报道抗肿瘤药物导致的心血管不良反应的发生率超过30%,心血管相关的毒性,被认为癌症幸存者中导致发病乃至死亡的第二大原因”
心血管毒性是癌症治疗的主要并发症。急性暴露于化疗药物或者抗肿瘤药物,可能直接影响心脏的离子通道功能,导致心脏兴奋性紊乱和心律失常;长时间作用,则可能会引起器质性的结构变化,发展出心室功能障碍和心力衰竭。
癌症治疗导致的心血管相关的后遗症是多样的,包括了:充血性心力衰竭、心律失常、心肌炎、左室射血分数(LVEF)下降、高血压、静脉、动脉血栓、外周动脉疾病、肺动脉高压、血管痉挛、蛋白尿、加速动脉粥样硬化和代谢紊乱等等。
风险和收益是药物开发, 尤其是肿瘤类药物、孤儿类药物开发需要去仔细权衡的:
“The threshold for toxicity may be different for a first-in-class therapy for a cancer type that has a poor prognosis and has few existing treatment possibilities versus a later-generation drug for a cancer with multiple existing therapies and a generally good prognosis”
伴随本土抗肿瘤类新药研发的井喷,我们相信此类药物的心血管安全性会是越愈来愈需要关注的问题,监管侧的要求也会不断规范、严谨。FDA的科学家明确指出
“Cardiovascular toxicities that are identified with new cancer therapies must be juxtaposed against the prognosis of cancer, the availability of existing therapies in the same class (for the same cancer), and the net benefit of therapy. The threshold for toxicity may be different for a first-in-class therapy for a cancer type that has a poor prognosis and has few existing treatment possibilities versus a later-generation drug for a cancer with multiple existing therapies and a generally good prognosis”
对于抗肿瘤药物而言,一个特别的挑战是,将心血管安全性研究结果纳入早期肿瘤临床实验。此类试验通常涉及少量参与者,并且可能采用单臂设计,因此很难确定疗效是否由药物引起;此外,在早期临床研究包括first-in-human study,部分患者面临心血管疾病的固有风险相对较高 或者 可能已经接受过与心血管并发症相关的治疗。另一个挑战是,在通常以亚治疗剂量作为起始的早期试验中需要剂量爬坡,这也使得评价化合物在这些患者中安全性和有效性遇到了问题。在2019年进行的一项关于TK抑制剂的回溯性研究中,发现有三分之一的患者在接受TK抑制剂后,出现了不同程度的QT延长。作者建议接受TK抑制剂治疗的癌症患者,需要接受持续的心电图监测。
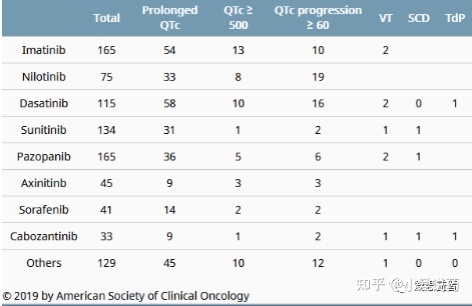
(https://ascopubs.org/doi/abs/10.1200/JCO.2019.37.15_suppl.3033)
在临床阶段,抗肿瘤药物潜在的心血管风险需要仔细的设计,观察和分析。也已经获得了人们的重视。伴随药物研发成本的不断飙升,在药物开发的早期,采用管控心血管风险的策略就变得越来越重要。那么,在临床前,有哪些工作可以帮助人们更好地管理抗肿瘤药物在心血管系统中的潜在风险呢?
Part-2:临床前研究, 在抗肿瘤药物的心脏安全性评价中扮演的角色。
随着人们对抗肿瘤药物具有的心血管毒性认识的不断深入,临床前研究越来越多地被用来对在研抗癌药药的心脏毒性进行早期评价。此外,也用于探究已有抗癌药物导致心血管毒性的机制。
在临床前研究中,体外实验或者体内实验(in vitro or in vivo)在不同的研究阶段,承担着了不同的作用。可以说前者在于风险确认(Hazard identification),后者着重于相应的风险测评(More aligned with risk assessment)一般而言,早期的筛选研究,设计到包括高通量读取在内的体验实验(例如:基于Qpacth检测hERG通道);体内的安全药理学(急性功能性影响)以及侧重于长期效应和器质性改变的毒理学研究。体外实验和离体实验,主要关注于药物在细胞(心肌细胞)或离体(离体组织或Langendorff心脏)模型的急性效应。相比之下,体内研究侧重于动物模型的长期效应。
目前,人源多能干细胞诱导的心肌细胞 (hiPS-CM) 被用于体外心脏毒性评价。具体的实验种类,可以包括如下几个几种:
1. 抗肿瘤药物导致的细胞毒性:e.g. TKI-Induced Cytotoxicity
2.抗肿瘤药物导致的致心律失常作用:可以利用传统的膜片钳或者微电极列阵的技术手段,主要关注点 delayed repolarization,EDA,conduction , altered spontaneous beating等等
3.抗肿瘤药物导致的对收缩力的影响:Contractile functions of hiPSC-CMs, 可以使用Impedance assay进行评价
4.结合生物标志物测量:cTnl, cTnT, (cardiac troponins)FABP3,以及 Myl3,这些生物标记物
可用于临床前安全评估研究中确认心肌结构的损伤。
此外,在离体实验中, 基于Langendorff系统的心脏灌流检测,可以提供一个综合性的心脏毒性评价, 测评的参数可以包括心率,心电图,左心室内压以及血流动力学等, 为后续体内乃至临床实验的开展,提供了有力参考。
Cardio-oncology是最近发展起来的心脏病学领域,旨在降低抗肿瘤药物导致的心血管疾病发病率以及由此导致的死亡,提高癌症幸存者的生存质量。癌症患者的生存率一直在不断上升,主要是因为新的、更有效的和有针对性的疗法的出现。然而,许多新疗法以及蒽环类等一些较老的化疗方案,都具有潜在的心脏毒性。心脏毒性对癌症患者的愈后有着极为不利繁荣影响,因此其预防和治疗抗肿瘤药物导致的心血管疾病具有高度的现实意义。
Ref:
1.Seltzer JH, Gintant G, Amiri-Kordestani L, Singer J, Koplowitz LP,Moslehi JJ, Barac A, Yu AF. Assessing cardiac safety in oncologydrug development. Am Heart J. 2019 Aug; 214:125-133.
2.PhRMA. List of. Medicines in development for cancer. 5 2018;30: 2018
https://www.phrma.org/report/list-of-2018-medicines-in-development-for-cancer.
3.IQVIA Institute Report. Global Oncology Trends. Innovation,expansion,anddisruption.52018;
24:2018https://www.iqvia.com/institute/reports/global-oncology-trends2018.
4.Barac A, Murtagh G, Carver JR, et al. Cardiovascular health of patients with cancer and cancer
survivors: a roadmap to the next level. J Am Coll Cardiol. 2015;65:2739 46
5.Risk of QTc interval prolongation among cancer patients treated with tyrosine kinase inhibitors.
Anan Abdelmoti Abu Rmilah, Grace Lin, and Joerg Herrmann Journal of Clinical Oncology 2019 37:15_suppl, 3033-3033
6.Sharma A, Burridge PW, McKeithan WL, Serrano R, Shukla P, Sayed N, Churko JM, Kitani T,
Wu H, Holmström A, Matsa E, Zhang Y, Kumar A, Fan AC, Del Álamo JC, Wu SM, Moslehi JJ,
Mercola M, Wu JC. High-throughput screening of tyrosine kinase inhibitorcardiotoxicity with human induced pluripotent stem cells. Sci Transl Med. 2017 Feb 15;9(377):eaaf2584.
7.Adamcova M, Skarkova V, Seifertova J, Rudolf E.Cardiac Troponins are Among Targets of Doxorubicin-InducedCardiotoxicity in hiPCS-CMs. Int J Mol Sci. 2019 May 29;20(11):2638.
5.结合生物标志物测量:cTnl, cTnT, (cardiac troponins)FABP3,以及 Myl3,这些生物标记物可用于临床前安全评估研究中确认心肌结构的损伤。
关于爱思益普
爱思益普成立于2010年,专注于基于靶点的先导化合物筛选和优化,以及中枢神经系统和心血管系统新药发现服务。公司批量构建了新药筛选的靶点和筛选技术,包括400多个激酶、100多个离子通道、100多个G蛋白偶联受体和40多个核受体靶点的药物筛选及早期成药性评价平台。爱思益普还建立了激酶谱筛选,体外脱靶效应靶点谱筛选,心脏安全性筛选等特色的脱靶效应体外筛选平台,致力于以高效、专业的服务,帮助新药研发企业快速有效地推进新药研发项目。

邮箱:Services@ice-biosci.com
网址:http://www.ice-biosci.com
地址:北京市亦庄经济开发区科创十三街18号院16号楼

扫一扫关注
爱思益普公众号


业务咨询
北京
业务咨询专线:010-6780-9840
联系地址:北京市经济技术开发区科创十三街18号院锋创科技园16号楼
上海
业务咨询专线:010-6780-9840
联系地址:上海市浦东新区蔡伦路780号新技术推广大楼3E5O室
徐州
业务咨询专线:010-6780-9840
联系地址:江苏省徐州市云龙区淮海文博园 二号楼2层
贵州
业务咨询专线:010-6780-9840
联系地址:贵州省贵阳市南明区龙岭路50号 欧美医药产业园一期2号楼



