News Detail
 来源:本站
来源:本站
 浏览量:13639
浏览量:13639
离子通道作为细胞膜上重要的功能性蛋白,调控着钠、钾、钙等离子的跨膜转运,在神经信号传导、心肌收缩、激素分泌等生理过程中发挥着不可替代的作用。据统计,约15%的已上市药物直接作用于离子通道靶点,这一比例在神经系统和心血管疾病治疗领域更是高达20%以上。随着药物研发向精准化方向发展,离子通道检测技术已成为创新药开发的关键支撑平台。
膜片钳技术被誉为离子通道研究的"金标准",其原理是通过玻璃微电极与细胞膜形成高阻封接(GΩ级),精确记录单离子通道的电流变化。如下图所示,爱思益普采用先进的膜片钳技术平台,可精确测定化合物对离子通道的抑制活性,获得IC50值和希尔系数等关键参数。传统手动膜片钳虽然数据精度高,但通量极低,每天仅能完成数个细胞的记录,难以满足现代药物筛选的需求。自动化膜片钳技术的出现彻底改变了这一局面,以QPatch、SyncroPatch为代表的自动化平台可实现48-384通道平行记录,日筛选量突破数千个化合物,效率提升近百倍。
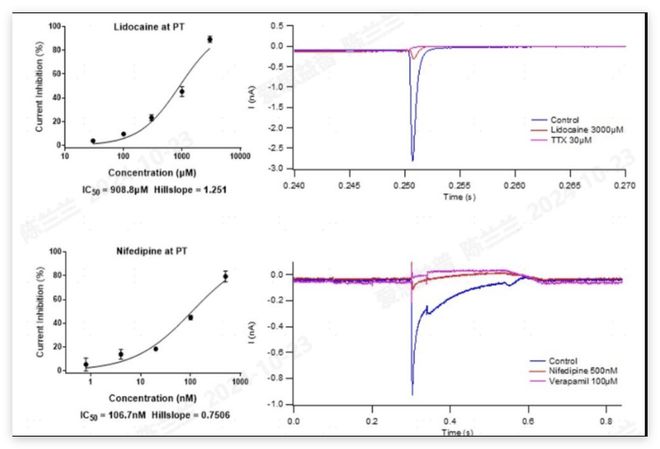
在心脏安全性评价领域,hERG钾通道检测已成为药物临床前研究的必检项目。hERG通道介导心肌动作电位复极化过程,药物对其抑制可导致QT间期延长,甚至诱发致命性尖端扭转型室性心动过速。国际协调理事会(ICH)S7B指南明确要求,新药临床试验申请(IND)前必须提交hERG安全性评价数据。自动化膜片钳系统可在生理温度(37℃)条件下精确测定化合物对hERG通道的半数抑制浓度(IC50),检测灵敏度达皮安级(pA),数据变异系数低于5%,为心脏毒性风险评估提供可靠依据。
电压门控钠通道(Nav)家族是疼痛治疗的重要靶点。Nav1.7、Nav1.8等亚型主要表达于背根神经节感觉神经元,在慢性疼痛状态下功能显著上调。通过构建稳定表达特定Nav亚型的细胞系,结合自动化膜片钳检测,可高通量筛选具有亚型选择性的抑制剂。这种选择性抑制策略可有效阻断病理性疼痛信号传导,同时避免对正常神经功能的影响,显著提高镇痛药物的安全性窗口。
钙通道(Cav)在神经递质释放和心肌兴奋-收缩耦联中起关键作用。Cav2.2亚型是N型钙通道的主要组成部分,其抑制剂已用于治疗慢性疼痛。通过膜片钳技术精确测定化合物对Cav各亚型的选择性,可指导药物分子结构优化,降低对心血管系统的不良影响。此外,钙通道阻滞剂在高血压、心绞痛等心血管疾病治疗中广泛应用,相关检测需求持续增长。
随着光遗传学、人工智能等技术的融合应用,离子通道检测正朝着更高通量、更智能化的方向发展。光诱导电生理学(LiEp)平台通过光遗传学工具实现毫秒级膜电位调控,可在单细胞水平动态监测药物与通道的相互作用。AI辅助信号分析算法则能自动识别异常电生理信号,将数据分析效率提升30%以上。这些技术创新为离子通道药物的快速发现提供了强大工具,推动着精准医疗时代的到来。

扫一扫关注
爱思益普公众号


业务咨询
北京
业务咨询专线:010-6780-9840
联系地址:北京市经济技术开发区科创十三街18号院锋创科技园16号楼
上海
业务咨询专线:010-6780-9840
联系地址:上海市浦东新区蔡伦路780号新技术推广大楼3E5O室
徐州
业务咨询专线:010-6780-9840
联系地址:江苏省徐州市云龙区淮海文博园 二号楼2层
贵州
业务咨询专线:010-6780-9840
联系地址:贵州省贵阳市南明区龙岭路50号 欧美医药产业园一期2号楼



