News Detail
 来源:2026-04-28 16:11:47
来源:2026-04-28 16:11:47
 浏览量:16709
浏览量:16709
传统药物研发遵循「占据并抑制」的占位驱动模式,要求小分子药物必须具备高亲和力结合口袋,这天然限制了可成药靶点的范围——据统计,人类基因组编码的约2万种蛋白中,仅 15% 具备传统意义上的可成药性。靶向蛋白降解(Targeted Protein Degradation, TPD)技术的出现彻底颠覆了这一范式。PROTAC(蛋白水解靶向嵌合体)与分子胶(Molecular Glue)通过劫持细胞自身的泛素-蛋白酶体系统,将靶蛋白标记为“垃圾并清除”,实现了从“抑制功能”到“消除蛋白”的策略跃迁。
这一技术突破的临床价值正在加速兑现。2024 年,全球首款 PROTAC 药物 ARV-471 进入 Ⅲ 期临床试验;2025 年,Kymera 公司的 KT-621 成为全球唯一进入临床阶段的口服 STAT6 降解剂,在中重度特应性皮炎患者中展现出优于传统生物制剂 dupilumab 的疗效。与此同时,分子胶药物也在血液肿瘤领域取得突破,来那度胺等免疫调节酰亚胺类药物(IMiDs)年销售额超过百亿美元,验证了 TPD 技术的商业化潜力。
然而, TPD 药物的开发复杂度远超传统小分子。 PROTAC 分子通常分子量达 700 - 1200 Da ,跨越“类药性五规则边界”,其溶解性、渗透性及代谢稳定性面临独特挑战;分子胶虽分子量较小(约 500 Da ),但作用机制隐蔽,需要精准调控蛋白-蛋白相互作用( PPI ),设计难度极高。在这一背景下,专业化 CRO 的技术赋能成为创新药企突破瓶颈的关键。
爱思益普生物科技股份有限公司凭借十余年靶点驱动药物发现的深厚积累,构建了覆盖 TPD 研发全周期的“靶点验证-复合物表征-细胞功能评价-成药性优化-临床前申报一体化平台。
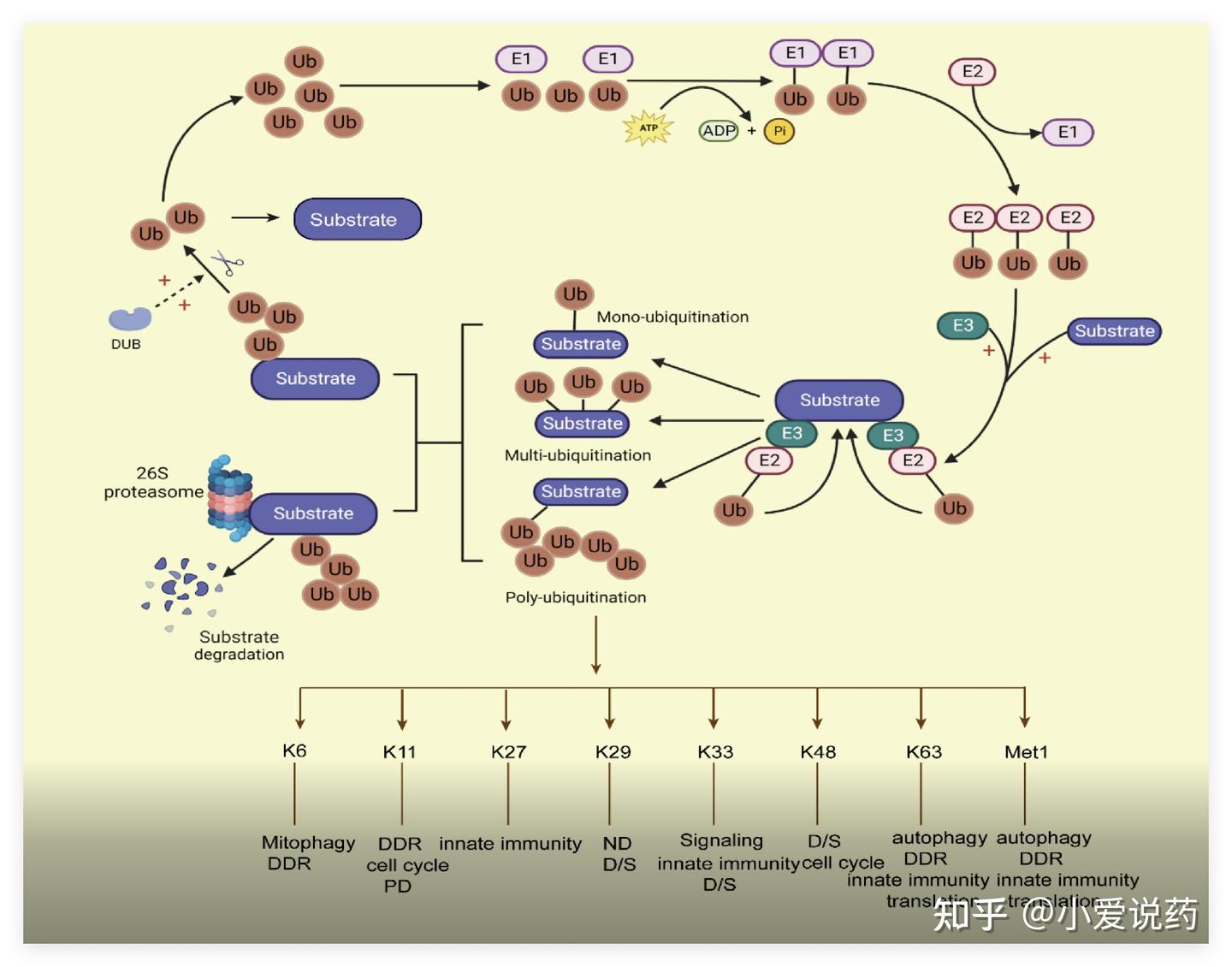
一、靶点验证体系: TPD 研发的基石
靶点验证是 TPD 研发的基石,决定了后续研究的方向与成败。爱思益普构建了以 700+ 高质量靶标蛋白库为核心的靶点验证体系,涵盖 STAT 家族(STAT3/6)、KRAS、VAV1、BRD4、EZH2、IKZF1/3 等热门 TPD 靶点,为全球药企提供坚实的研发支撑。
平台采用多技术组合实现靶点可降解性的系统性评估:
⏰️ TR-FRET(时间分辨荧光共振能量转移)技术模拟靶蛋白与相关受体或配体的结合场景,实现小分子抑制剂的高通量亲和力筛选。在 STAT6 降解剂 KT-621 的研发中,平台通过 TR-FRET 技术模拟 STAT6 与 IL-4R 的结合场景,为后续 PROTAC 分子设计提供了关键的亲和力数据。
⏰️ 光谱位移法(SPS)则评估 PROTAC 分子与 E3 连接酶(如 CRBN、VHL)的结合能力,以及“E3 连接酶-PROTAC-靶点”三元复合物的组装效率。
⏰️ SPR(表面等离子共振)技术对化合物与靶蛋白家族的结合动力学进行精准表征,计算结合速率常数(Ka)、解离速率常数(Kd)及平衡解离常数(KD),为分子优化提供动力学层面的深度数据。
这种多技术整合的验证策略具有显著的协同效应。TR-FRET 提供亲和力信息,SPS 揭示复合物稳定性,SPR 解析动力学特征,三者结合可全面评估靶点的可降解性潜力。在某 KRAS 突变项目中,平台通过该体系发现 KRAS G12C 突变体与特定 E3 连接酶存在天然亲和力,为设计选择性降解剂提供了理论依据。
平台还建立了靶点家族选择性筛选模型。针对 STAT 家族高度同源的特点,平台提供 STAT1/2/3/4/5/6 的选择性筛选服务,确保降解剂对目标靶点的特异性。在 KT-621 研发中,该平台验证了其对 STAT6 的选择性降解活性,避免了泛 STAT 抑制带来的免疫抑制副作用。
二、复合物表征平台:三元复合物稳定性的精密解码
PROTAC 能否起效,取决于「目标蛋白-PROTAC-E3 酶」三元复合物的稳定性与几何构型。这一「分子黏合」过程的效率直接决定降解活性,因此三元复合物的精准表征成为 TPD 研发的核心环节。爱思益普整合光谱位移法(SPS)、均相时间分辨荧光(HTRF)及表面等离子共振(SPR)三大技术,构建了业界领先的三元复合物表征体系。
三元复合物表征体系:
💧 光谱位移法(SPS)通过检测分子间相互作用引起的光谱变化,灵敏反映 PROTAC 分子与 E3 连接酶的结合情况。该方法无需标记,避免了荧光标签对分子构象的潜在干扰,能够真实反映复合物形成的亲和力与稳定性。在 STAT6 降解剂 KT-621 的研发中,平台采用 SPS 技术评估 PROTAC 分子与 CRBN 的结合亲和力,结合 HTRF 技术验证三元复合物的组装效率,最终实现 pM 级亲和力的精准调控。
💧 HTRF 技术基于荧光共振能量转移原理,通过供体荧光团与受体荧光团的空间邻近变化定量分析三元复合物形成。平台优化了供体/受体标记策略,将 CRBN 与靶蛋白分别标记,PROTAC 分子的加入导致荧光信号增强,信号强度与三元复合物浓度呈正相关。这种设计实现了高通量筛选,单次实验可评估数百种 PROTAC 分子的三元复合物形成能力。在某 BRD4 降解剂筛选项目中,平台通过 HTRF 技术从 5000 余种化合物中快速识别出高效三元复合物形成剂,将先导化合物发现周期缩短50%。”
💧 SPR 技术提供动力学层面的深度解析。通过将靶蛋白或 E3 连接酶固定于芯片表面,实时监测 PROTAC 分子的结合与解离过程,获取 Ka、Kd 及 KD 等动力学参数。在某 STAT3 降解剂项目中,平台仅通过 SPR 结合动力学分析与 HiBiT 降解检测模块,即完成关键机制验证,研发周期缩短 40%。这种“动力学+功能性”的模块化组合,显著提升了研发效率并降低了成本。
平台还建立了分子胶的复合物表征能力。与 PROTAC 的双功能分子设计不同,分子胶为单一小分子,通过诱导、稳定或增强靶蛋白与 E3 连接酶之间的相互作用实现降解。平台开发了二元/三元复合物检测技术,精准锁定分子胶诱导的蛋白相互作用,明确分子胶、靶蛋白、E3 连接酶三者的结合关系。在诺华 VAV1 分子胶降解剂的临床前研究中,平台通过该技术验证了分子胶对 VAV1-CRBN 相互作用的诱导能力,为后续优化提供了结构基础。
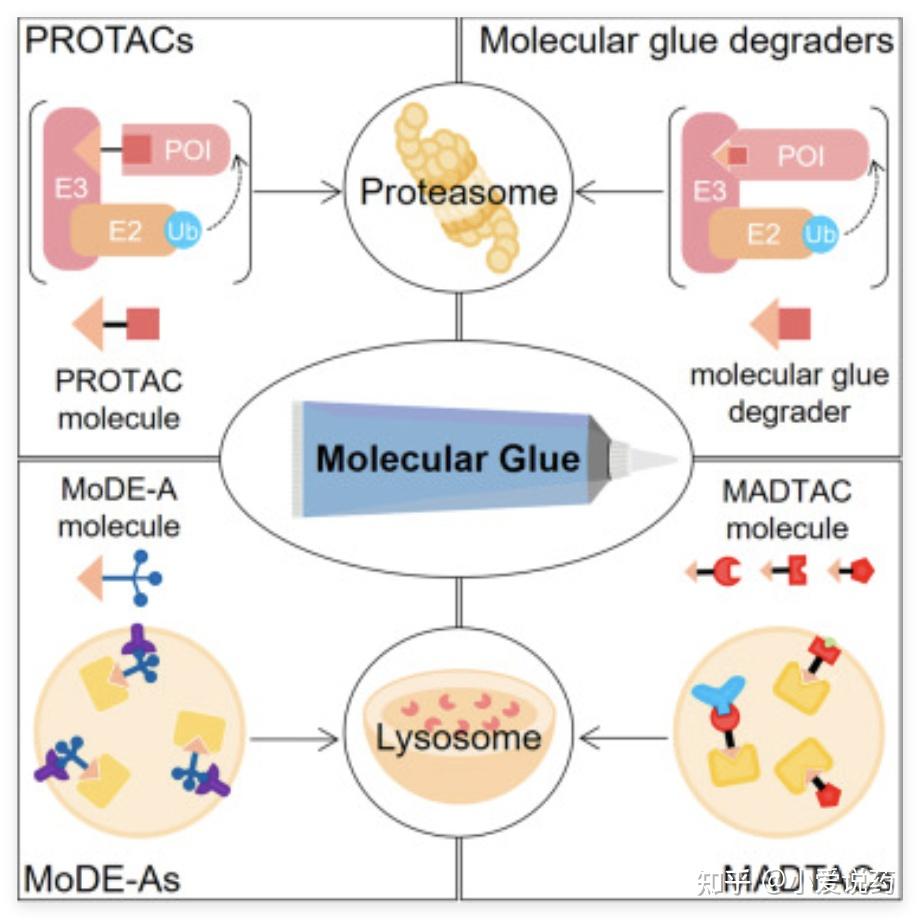
三、细胞功能评价:从蛋白降解到信号通路的全维度验证
细胞水平功能评价是连接分子机制与体内药效的关键桥梁。爱思益普构建了覆盖靶蛋白降解检测、信号通路抑制评估及临床相关性验证的多维度细胞模型体系,为 TPD 药物提供全链条评价。
多维度细胞模型体系:
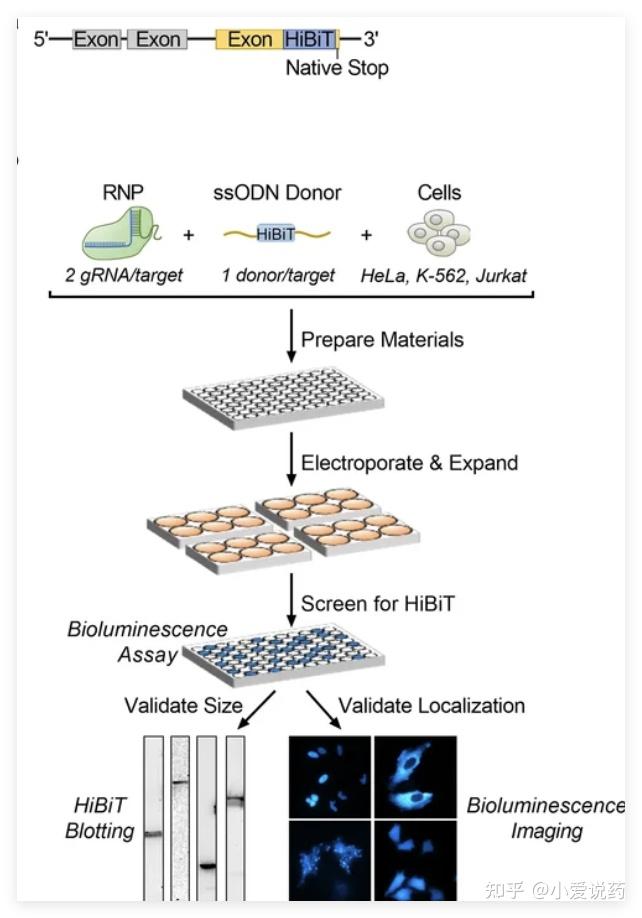
💡 HiBiT(High Bioluminescence Tag)技术是平台的标志性工具。通过 CRISPR-Cas9 基因编辑将 HiBiT 标签(仅 11 个氨基酸)精准敲入内源性靶蛋白基因座,构建报告基因细胞系,实现蛋白降解的实时、定量、高通量监测。检测时加入互补肽 LgBiT 及荧光素底物,两者结合形成完整荧光素酶产生发光信号;当 PROTAC 诱导靶蛋白降解时,HiBiT 标签随靶蛋白一同被降解,发光信号减弱,信号衰减程度直接反映降解效率。平台已构建 STAT6 HiBiT A549、Jurkat STAT6 HiBiT-KI、BRD4 HiBiT 等多种敲入细胞系,检测灵敏度达 pM 级别。相比传统 Western Blot,HiBiT 技术检测速度快(3 小时 vs 2 天)、定量准确、数据可重复,且支持高通量筛选。
💡 Western Blot作为检测靶蛋白降解的金标准,与HiBiT技术形成互补。平台利用LI-COR公司的Odyssey DLx双色红外荧光成像平台,可在细胞微孔板中进行In-cell Western assay(ICW)分析,结合Western Blot的特异性和ELISA的可重复性与高通量特性。在某BTK降解剂项目中,平台通过Western Blot验证组织水平的靶蛋白清除情况,确认降解效率达85%以上。
💡 信号通路抑制评估是细胞功能评价的另一维度。平台基于 HEK293-STAT6-Luc2p 报告基因细胞系,通过荧光素酶活性检测化合物对 STAT6 信号通路的抑制能力。在 KT-621 研发中,该模型验证了其对 IL-4/13 通路的完全阻断作用,效力优于传统生物制剂 dupilumab。平台还开发了人 PBMC 及 B 细胞功能检测体系,通过检测 CCL17 释放量与 CD23 表达水平,结合流式细胞术检测 STAT6 磷酸化抑制情况,全面评估化合物的临床相关活性。
💡 蛋白质组学脱靶研究技术可揪出潜在脱靶风险,确保药物特异性。在 BRD4 降解剂研发中,平台通过质谱分析发现某候选分子对 CBP/p300 的非预期降解,经结构修饰后选择性提升至 95% 以上。这种“降解效率+选择性+通路抑制”的多维度评价体系,显著提高了先导化合物的成药性。
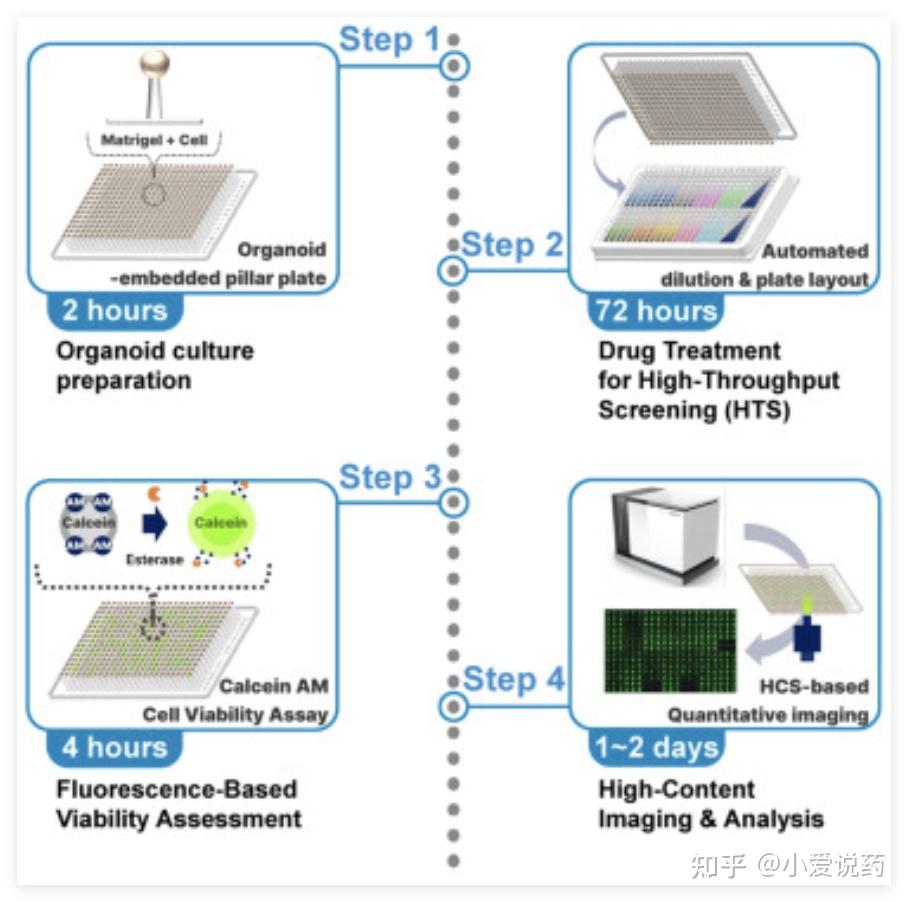
四、分子胶筛选平台: PPI 调控网络解析的创新引擎
分子胶作为 TPD 领域的新兴技术,通过诱导蛋白质间相互作用(PPI)实现靶蛋白降解,为攻克「不可成药」靶点提供了新思路。与 PROTAC 的双头结构不同,分子胶是单个小分子(约 500 Da),像「胶水」一样把两个原本不结合的蛋白黏在一起,具有分子量小、口服生物利用度高、成药性好的优势,但设计难度大,需要精准调控蛋白相互作用。
爱思益普的分子胶筛选平台整合了三大核心技术,构建了独特的「PPI 调控网络解析体系」。蛋白质组学分析技术鉴定与靶蛋白相互作用的关键伴侣分子,为分子胶设计提供靶点信息。在针对 IKZF1/IKZF3 的分子胶研发中,平台通过该技术发现可稳定蛋白相互作用的分子胶化合物,降解活性较传统方法提升 3 倍以上。CRISPR-Cas9 基因编辑技术构建内源性表达细胞模型,避免外源转染的过度表达假象,确保数据贴近生理真实。高通量筛选技术则实现化合物库的快速评估,单次可筛选数万种分子胶候选物。
平台建立了多层次验证体系确保分子胶的特异性与有效性:
📚 二元/三元复合物检测技术精准锁定分子胶诱导的蛋白相互作用;
📚 细胞内三元复合物形成验证动态追踪“黏合”效果;
📚 JESS 和 HiBiT 技术量化降解效率,确保疗效可评估。
📚 蛋白质组学分析揪出脱靶风险,确保药物特异性。
JESS 技术相比传统 Western Blot 具有样品需求量低、检测速度快、全程自动化标准化、数据可重复等优势。在 VAV1 靶点研发中,平台建立的专属检测体系可同时监测靶蛋白降解与细胞功能变化,通过检测 T 细胞活化标记物 CD69 的表达水平,验证分子胶对 VAV1 信号通路的抑制作用。诺华 VAV1 分子胶降解剂的临床前研究验证了该体系的有效性——动物实验显示炎症指标下降 70%,且未出现传统 JAK 抑制剂的血栓风险。这一成果得益于平台对分子胶诱导的蛋白相互作用的精准锁定及对结合效果动态的追踪。
五、成药性优化与 DMPK:PROTAC 药物的临床前转化引擎
PROTAC 分子的大分子量与复杂结构特征对成药性提出了独特挑战。爱思益普构建了 PROTAC 专属的体外 ADME 与体内 PK 评价体系,通过 LC-MS/MS 高灵敏度检测技术,助力筛选药代特性优良的候选分子。
体外 ADME 评价涵盖透膜能力(PAMPA 或 Caco-2 模型)、溶解度(动力学与热力学溶解度)、血浆蛋白结合率、肝微粒体稳定性及 CYP 酶代谢特征。在某 STAT6 降解剂项目中,平台通过肝微粒体稳定性试验预测候选分子半衰期达 12 小时,为后续口服剂型设计提供了关键数据。针对 PROTAC 分子常见的低渗透性问题,平台建立了平行人工膜渗透性(PAMPA)筛选模型,快速识别具有适宜渗透性的先导结构。
体内 PK 研究方面,平台开发了适用于 PROTAC 分子的生物分析方法。由于 PROTAC 分子分子量大、结构复杂,传统生物分析方法面临灵敏度不足、特异性差等挑战。平台通过优化样品前处理流程(蛋白沉淀、固相萃取)和 LC-MS/MS 检测条件(选择反应监测 SRM 模式),实现了血浆、组织等多种生物基质中 PROTAC 分子的准确定量。在某 BTK 降解剂研发中,平台通过体内 PK 研究绘制了完整的血药浓度-时间曲线,计算出 AUC、Cmax、Tmax 等关键参数,为给药方案优化提供了科学依据。
平台还整合了体内药理模型验证成药性。特应性皮炎、哮喘、肠炎等疾病模型模拟人体病理过程,使药效验证更贴近真实临床场景。在 KT-621 的临床前研究中,平台通过特应性皮炎模型验证了显著的炎症指标改善,数据直接支持了Ⅰ期临床试验设计。这种「体外 DMPK 优化-体内药效验证-机制确证」的闭环体系,显著缩短了 TPD 药物的研发周期并降低了转化风险。
爱思益普的 TPD 平台并非简单的技术集合,而是覆盖药物研发全周期的整合服务体系:
🖥️ 在早期发现阶段,700+ 蛋白库支持靶点可降解性评估;TR-FRET、SPR、SPS 等技术组合实现高通量筛选;CRISPR-Cas9 基因编辑构建内源性敲入细胞系。
🖥️ 在优化验证阶段,HiBiT 细胞系实时监测降解效率;流式细胞术检测信号通路抑制;蛋白质组学脱靶研究确保特异性。
🖥️ 在临床前开发阶段,DMPK 筛选评价覆盖吸收、代谢、毒性全维度;体内药理平台拥有多种疾病模型;IND 申报支持提供符合 GLP 规范的数据包。
平台的技术标准化与模块化设计提升了服务效率与数据可靠性。实验设计采用盲法设置,设备校准通过第三方认证,数据分析实现自动化处理。在 BRAF V600E 突变黑色素瘤项目中,三次独立筛选的 IC50 值重复性误差小于 15%,数据直接用于化合物结构优化。平台将靶点验证、复合物表征、细胞功能评价等环节拆分为独立模块,客户可根据需求灵活组合。某药企在研发 STAT3 降解剂时,仅选用平台的 SPR 结合动力学分析与 HiBiT 降解检测模块,即完成关键机制验证,研发周期缩短 40%。
这种「模块化+标准化」的模式降低了中小型药企的研发门槛。通过提供从靶点验证到临床前申报的全链条服务,爱思益普的平台正在加速突破性降解疗法的临床转化。目前,该平台已支持全球药企完成数十项 TPD 项目的 IND 申报,成为行业创新的重要推动力。随着 KT-621 等分子的临床推进,TPD 技术正从实验室走向临床,为数亿炎症性疾病与肿瘤患者点燃希望之光。
结语:构建 TPD 研发的中国方案
靶向蛋白降解技术作为药物研发领域的范式革命,正在重塑「不可成药」靶点的治疗格局。爱思益普以 700+ 高品质蛋白库为基石,以多技术整合平台为支撑,以全链条服务体系为纽带,构建了独具特色的TPD研发赋能生态。从靶点验证的精准定位,到复合物表征的深度解析;从细胞功能的多维评价,到成药性的系统优化;从PROTAC的双功能分子设计,到分子胶的PPI调控创新——平台的技术能力覆盖了TPD研发的每一个关键环节。
2026 年,爱思益普计划推进 IPO 申报,以技术为擎助力全球创新药研发进程提速。随着双特异性 PROTAC、双药 ADC 等新一代技术的成熟,靶向蛋白降解药物将在更多疾病领域发挥变革性作用。爱思益普将持续投入技术创新,与合作伙伴共同推动 TPD 研发进入新纪元,为全球患者提供更多、更好的治疗选择!